
����ѧ��˼1��1>���л�ѧ>����

��Ԫ���Ծ�حѧ��֪ʶͬ��ح������ĩ����
�������л�ѧ��ʵ���ԱȽ�ǿ��ѧ�ƣ�ͬѧ����Ҫ��������Ļ�ѧ����ʽ��ʵ������ѧ�����ȣ���Щ����ʮ�����ƣ��������֣����ͬѧ�Ǹ�Ҫ��ѧ������Щ֪ʶ�㡣��ѧʵ���Ҹ߿������ѵ㣬Ϊ�˰���ͬѧ��ѧ�ø��л�ѧʵ�鲿�֣����ǿ��߿�Ƶ��С��Ϊͬѧ���������������л�ѧ̽����ʵ����Ŀ��ϣ����ͬѧ�Ǵ���һ���İ�����
�����������л�ѧ̽����ʵ����Ŀ(һ)
��������һģ28.(15��)ij���Ӷ�Na2SO3��AgNO3�ڲ�ͬPH�µķ�Ӧ����̽����
����(1)���Na2SO3��ҺPH=11��AgNO3��ҺPH=5������ˮ������ӷֱ��� (2)����PH��ʵ���¼���£�

�����������ϵ�֪��
����i.Ag2SO3����ɫ��������ˮ�����ڹ���Na2SO3����Һ ii.Ag2O���غ�ɫ��������ˮ���ܺ��ᷴӦ
�������Ʋ�a�а�ɫ����ΪAg2SO3�����ӷ���ʽ�� ���Ʋ�a�а�ɫ����ΪAg2SO4���Ʋ��������
����(3)ȡb��c�а�ɫ����������Na2SO3��Һ�У������ܽ⡣��ͬѧ���ʵ��ȷ���˰�ɫ��������Ag2SO4��ʵ�鷽���ǣ���ȡAg2SO4�������� ��Һ�У�δ�ܽ⡣ (4)�����˳���ϴ����Ϊȷ������ɣ�ʵ�����£� ��.��X�еμ�ϡ���ᣬ�����Ա仯
������.��X�м������ŨHNO3����������ɫ����
������.��Ba(NO3)2��Һ��BaCl2��Һ������з�Ӧ�����Һ��ǰ���ޱ仯�����߲�����ɫ����
������ʵ����Ŀ���� ��
�����ڸ�������������X�����ʺ�Ԫ������� �ۢ��з�Ӧ�Ļ�ѧ����ʽ��
����(5)��ͬѧ�ۺ�����ʵ�飬��������X��ԭ����Ϊ�������Ե���ǿ����ԭ����ǿ��ͨ����һ��ʵ��ȷ�������ֿ����ԣ�ʵ�����£�
����������Y�� ��
�����ڰ�ɫ����ת��ΪX�Ļ�ѧ����ʽ��
�����������л�ѧ̽����ʵ����Ŀ(��)
��������һģ28.(15��)ij������ͨ��ʵ�鷽����֤Fe2+�����ʡ� (1)��ͬѧ��ʵ��ǰ������Fe2+�� �ԣ���д���±���
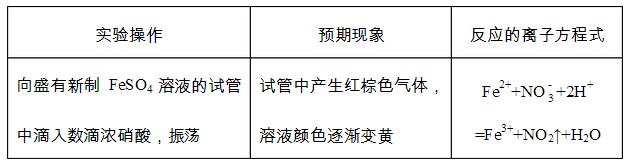
�������ձ��в�������ͬѧ����ʵ�顣�۲쵽Һ���Ϸ�������Ϊ����ɫ�����Թ�����Һ��ɫȴ��Ϊ����ɫ��
����Ϊ�˽�һ��̽����Һ�������ɫ��ԭ��ͬѧ��������ʵ�顣
����(2)��ԭ����FeSO4��Һ�ͷ�Ӧ����Һ�о�����KSCN��Һ��ǰ�߲����ɫ�����߱�졣
����������Ľ����� ��
����(3)��ͬѧͨ���������ϣ���Ϊ��Һ������ɫ������NO2��NO����Һ��Fe2+��Fe3+������Ӧ���õ��ġ�Ϊ�������ã���ͼװ��(�������Ѽ��飬β������װ����)����̽����

������.����a���ر�b����ʹ��װ���з�Ӧ��ʼ�۲쵽������Һ��Ϊ����ɫ����������Һ�����Ա仯��
������.����b���ر�a��һ��ʱ�����ֹͣ���з�Ӧ��
������.Ϊ�뢡��ʵ����ж��գ�������������ʹ���з�Ӧ�������۲쵽�������벽�袡����ͬ��
������ͭ������Ũ���ᷴӦ�Ļ�ѧ����ʽ�� ; ��װ���ҵ������� ; �۲��袢��Ŀ���� ; �ܸ�ʵ��ɵó��Ľ����� ��
����(4)��ͬѧ���½���(1)��ʵ�飬�۲쵽��Ԥ��������ʵ������� ��
�����������л�ѧ̽����ʵ����Ŀ��Ϊͬѧ�Ƿ����������ˣ������һ���ʲô����Ļ�����ֱ�Ӳ��������ѯ�绰��4000-121-121!��רҵ����ʦΪ�����!